01. Halmazállapotok jellemzői_Gázok
Megnézem a feladatlapot, a kitöltését
Aki meg hiányzott az óráról, az nézze meg a számolásokhoz a videós segédletet:
- ezeket az összefüggéseket kell ismerni
- ezek pedig a táblázatban található számolások
- itt pedig a szöveges feladatok, relatív sűrűség
Ezt tanultad 7. osztályban:
Nézd meg a videót, sokat segít a tanulásban:
Fontos megérteni: halmazállapot változás hőmérséklete addig nem változik, amig a halmazállapot átalakulás zajlik. Nézd meg a szimulációt!
Ez egy fontos feladat: MEGOLDOM!
Füzetvázlat:
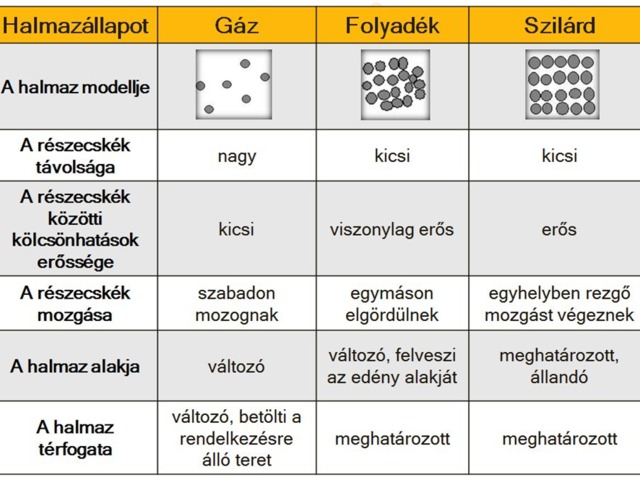
I.Ismétlés: Mi befolyásolja egy anyag halmazállapotát?
- Részecskék közti kötések:
- Ionos kötés à szilárd anyagok: ionrácsok
- Fémes kötés à szilárd anyagok: fémrácsok
- Kovalens kötés:
- Szilárd anyagok: atomrácsok (grafit, gyémánt)
- Molekulák, köztük lévő másodrendű kötések:
- Diszperziós (leggyengébb): apoláris molekulák közt
- Dipólusos: poláris molekulák közt
- H hidas (legerősebb): olyan molekulák közt, amiben H + F,O,N kötés van
- Állapotjelzők
- Hőmérséklet (T, mértékegység K, °C + 273 = K)
- Nyomás (p, mértékegység Pa)
II. Gázok
1. Jellemzői
- a részecskék közötti összetartó erő gyenge másodrendű kötés;
- részecskék tömege kicsi , hőmozgás sebessége nagy;
- rendelkezésre álló teret kitöltik
- ideális gázok részecskéinek térfogata elhanyagolható a gáz teljes térfogatához képest, és a részecskék közt nincs kölcsönhatás
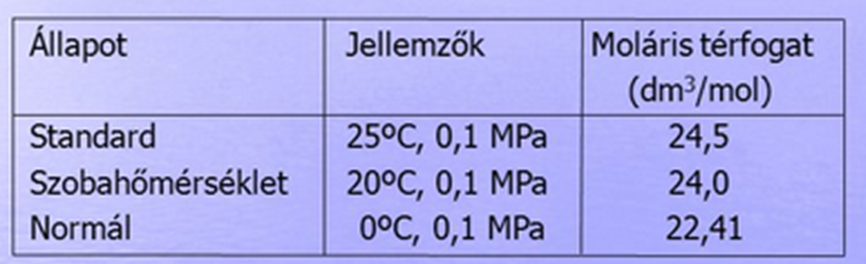
2. Gázok állapotai
3. Avogadro törvénye
Különböző gázok azonos hőmérsékleten és nyomáson ugyanakkora térfogatot töltenek be amennyiben anyagmennyiségük megegyező. (Ebből következő összefüggés: GÁZOKNÁL A MOLARÁNY MEGEGYEZIK A TÉRFOGATARÁNNYAL)
4. Gázok relatív sűrűsége: Megmutatja, hogy egy gáz egy másikhoz képest mekkora sűrűségű. Általában levegőhöz képest szoktuk nézni, aminél M=29g/mol.
(Relatív sűrűség jele d vagy:
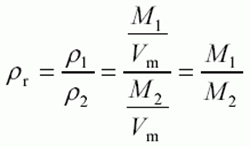
(Nézd meg a videót a kén-hexafluoridról, és a nemesgázokról!)
5. Diffúzió: hőmozgás, keveredés:
Kísérletek:
- Miért érezzük a szalmiákszesz szagát?
- Mi történik, ha sósavval hozzuk össze?
EMELT: II. Gázok állapotegyenlete
Bármelyik gázra, bármilyen hőmérsékleten vagy nyomáson érvényes összefüggés:
pV = nRT
- p = nyomás Pa
- V = térfogat, m3
- n = anyagmennyiség, mol
- T = hőmérséklet, K (273,1-el váltva!)
- R = 8,314 J/Kmol (egyetemes gázállandó)
Érdekességek
A csodálatos vákuum: Amitől igazán felforr a vérünk, és Galilei kísérlete: Mi a nehezebb, 1kg toll vagy 1kg vas?
Plazmaállapot, a 4. halmazállapot: ez lehet a jövő energiaproblémájának megoldása. Otthon is megvalósítható, de azért ne próbáld ki otthon!
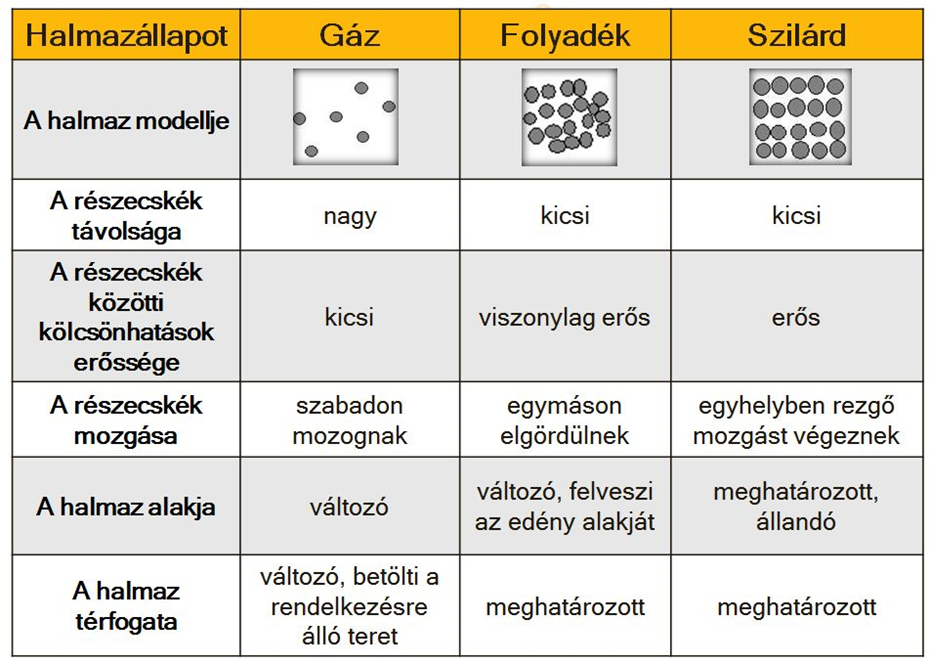
- Mi jellemező a gázokra/folyadékokra/szilárd anyagokra? (Rajzolj halmazmodellt, részecskék távolsága, részecskék közti kölcsönhatás, mozgás, alak, térfogat)
- Változik-e a hőmérséklete a víznek, miközben olvad benne a jég?
- Mitől függ egy anyag forráspontja?
- Gázok állapotai + állapotjelzők
- Tömeg-anyagmennyiség-moláris tömeg összefüggése
- Anyagmennyiség- részecskeszám- Avogadro szám összefüggése
- Térfogat- anyagmennyiség-moláris térfogat összefüggése
- Sűrűség-tömeg- térfogat összefüggése
TANULNI !!!! QUIZLET
Emelt szinten tudni kell a fontosabb gázok ipari és laboratóriumi előállítását: QUIZLET
És íme a DOLGOZAT!!!