2.4.1. Oxigén és az ózon
Ezt tanultuk 8. osztályban (ha emlékszel- akkor csak ismétlés, szinte ugyanaz a blogbejegyzés is. Az új LearningApps feladatok be vannak ágyazva a bejegyzésbe)
Honnan és hogyan tanulj?
Alapórára:
- tk + mf
- Alapismeretek - nyomtatható, world formátum, oxigén-ózon-víz-hidrogénperoxid
Emelt érettségire:
- Villányi tk. 187-188.o
- Megnézem a ppt-t! (Egészítsd ki a könyvet, ha új ismeretet találtál a ppt-ben!) + vévignézem a bejegyzést
- Learning Apps feladatok megoldása
- Quizlet - reakcióegyenletek begyakorlása (csak akkor fog menni, ha leírod!!!)
- Redmenta dolgozat megírása (csoportban megosztva)
- Szóbeli tétel kidolgozása / átgondolása
- Bejegyzés végén nézd meg a kísérleteket!
:
I. Kémiai részecskéi
Milyen kötéseket tud kialakítani?
- Teljes elektronleadással oxidionná alakul --> ionkötés
- Részleges elektronleadással molekuát képez --> kovalens kötés
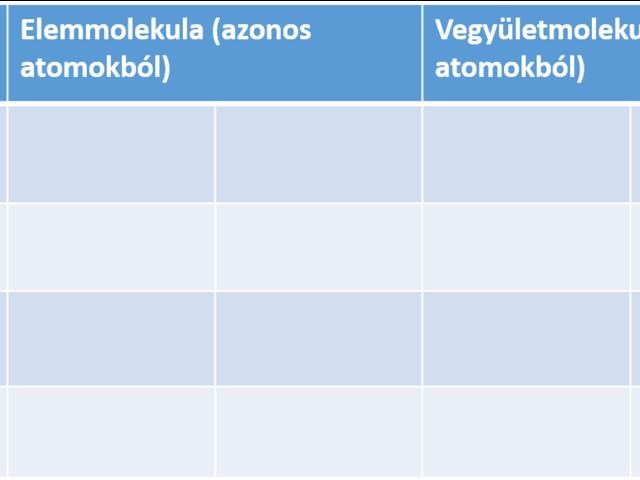
Rakjuk ki kalott modellből a következő molekulákat, majd egészítsük ki az alábbi táblázatot! (Kalott modell helyett használhatunk online molekulatervezőt is! MOLVIEW)
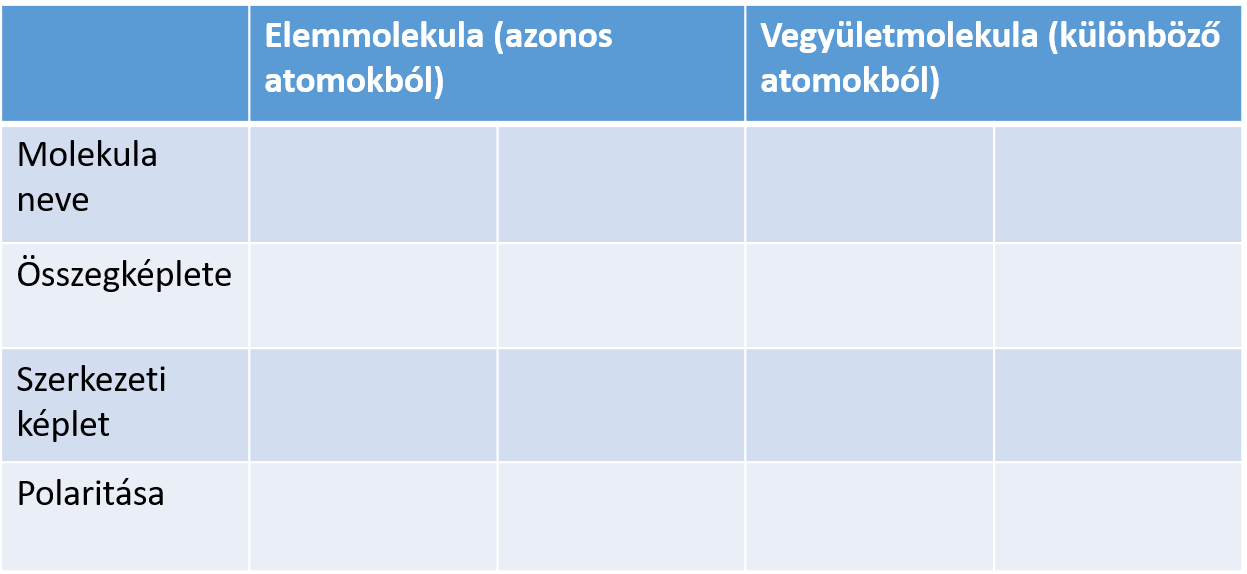
II. Fizikai tulajdonságok
Hasonlítsuk össze az oxigént és az ózont az alábbi feladat alapján, majd egészítsük ki a táblázatot!

III. Kémiai tulajdonságok
Írd fel a reakcióegyenleteket! Rendezd! Nevezd el a termékeket!
Nemfémekkel molekulákat képez:
- hidrogén + oxigén (Durranógáz reakció - nézd meg!)
- szén + oxigén
- kén + oxigén
Fémekkel ionvegyületeket képez:
IV. Előfordulás
Nézz körbe Montenegró északi részén a Fekete tó környékén! Milyen formában fordul elő az oxigén?
V. Előállítás
Emlékszel?
Laborban:
- Vízbontás
- Hipermangán hevítése
- Hidrogén-peroxid bomlása
Természetben: fotoszintézis
Ipar: levegő cseppfolyósítás
VI. Élettani jelentősége
VII. Felhasználás
Összefoglalás:
Filmajánló: Az egyetlen Föld - Az oxigén nyomában
Kísérletek
1. Oxigén előállítás, kimutatás
- VIDEÓ - hipermanán bomlása
2. Durranógázpróba
- VIDEÓ
- Cink+ sósav reakció, majd durranógáz próba
3. Kén égése
- VIDEÓ: Kénszalag égése (sajnos ne olyan jól /semennyire se látszik, hogy a kén kék lánggal ég. Mérgező kén-dioxid keletkezik (fülke alatt kellene végezni a kísérletet), ami vízben kénessavá alakul. A kísérlet szemlélteti a savas esső kialakulásának okát, az indikátor színváltozása mutatja a savasodást
- VIDEÓ: ebben szépen látszik a kék láng
4. Al oxidálódása, higany-kloridos oxidbontás után
5. Mg égése
6. Vas és alumíniumpor égése
4. Fotoszintézis oxigéntermelésének kimutatása
- VIDEÓ
- Átokhínárral
5. Növényi légzés és fotoszintézis
Emelt kísérletek: