2.3.1. Halogének
Ezt kellene tudnod: Ezt tanultad 8. osztályban - érdemes végignézni!
A leckéből megtudhatod:
- Miért kell tanfolyam a tisztítástechnológiai szakmunkásnak?
- Mit tartalamz a lejárt szavatosságú hipó?
- Semmelweis miért lett az anyák megmentője?
- Mire jó a jódtabletta? Miért kellett adni a lakosságnak Csernobilban?
Innen tanulj:
- Villányi tk: 178-181.o + feladatgyűjtemény
- Ppt-k: Halogének_2024
- Halogének feladatlap
- LearningApps feladatok
- És alighanem a legfontosab: reakcióegyenletek QUIZLET
- Redmenta dolgozat megírása (csoportban megosztva)
- Szóbeli tétel kidolgozása / átgondolása: itt a teljes szervetlent megtalálod, keresd meg a halogénes részt!
Füzetvázlat
Másold le a tálázatot a füzetedbe, majd a ppt alapján egészítsd ki! (Ne húzd meg előre a sorokat, mert van, ahova több dolgot kell írni)

Ezt a leckét az általános kémián tanult ismereteink alapján fogjuk egy KAhoottal átnézni. Amire emlékezned kellene:
- Hogyan tudjuk megállapítani egy adott elemről, hogy annak mi a vegyértékelektron-szerkezete?
- Honnan tudod megállapítani, hogy hányadik a vegyértékhéj?
- Honnan tudjuk a vegyértékelektronok számát?
- Mit jelent, hogy egy egy elem s, p vagy d mező eleme?
- Hogyan változik az EN a periódusos rendszerben?
- Honnan tudjuk meghatározni, hogy két atom közt milyen kötés jöhet létre?
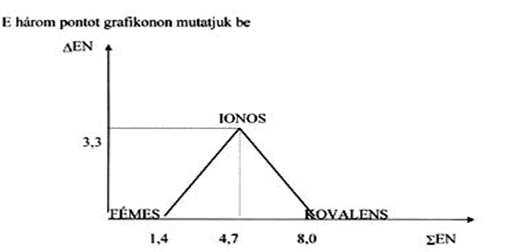
- Mitől függ a molekulák polaritása?
- Milyen másodrendű kötéseket ismersz? Mi a kialakulásuk feltétele?
- Hogyan határozzuk meg egy molekulában az atomok oxidációs számát?
- Hogyan változik az atomok és mérete a periódusos rendszerben?
- Mitől függ az anyagok standard halmazállapota?
- Hogyan tudjuk megmondani egy ismert összetételű gázról, hogy a levegőhöz képest mekkora a sűrűsége?
- Milyen anyagok oldódnak jól vízben?
- Milyen típusú reakciók a fémek+halogének reakciói a
- reakcióban részt vevő anyagok száma szerint?
- részecskeátmenet szerint?
- energiaváltozás szerint?
- Hogyan tudjuk megállapítani standardpotenciálja alapján egy vegyületről, hogy oxidálószer vagy redukálószer? Melyik a legjobb oxidálószer?
- Elektrokémia: Mit elektrolizáljunk és milyen körülmények közt, ha klórgázt szeretnénk előállítani?
Jöhet a KAHOOT!
Kísérletek
1. A jód apoláris és könnyen szublimál
- Jódgőz molekulái feloldódnak ujjlenyomatunk zsírrétegében --> ujjlenyomat vétel
- VIDEÓ
2. Jód oldódása különböző oldószerekben
- Oxigén tartalmú oldószer --> barna szín, oxigénmentes --> lila
- VIDEÓ
3. Klórgáz színtelenítő hatása
- VIDEÓ: színes virág elszíntelenedik
4. Halogének reakciója hidrogénnel
- VIDEÓ: a klórdurranógáz a vaku fényétől felrobban
- VIDEÓ (2 perctől): gázkeverék borszeszégővel berobbantva
5. Halogének reakciója fémekkel
- VIDEÓ: Na égése klórgázban
- VIDEÓ: izzó vasdrótot teszünk klórgázba
- VIDEÓ: Al és jód reakciója, vízkatalizátorra
- VIDEÓ: Mg+brómos víz
6. Halogének reakciója egymással
- VIDEÓ: a klórgáztól a KI-os papír megbarnul, mert jód keletkezik, ami KI-ban oldva Lugol
7. Klórgáz előállítás
Érdekességek:
- Jódóra - VIDEÓ
EMELT KÍSÉRLETEK:
- 2.: Aceton, víz, benzin azonosítása jóddal VIDEÓ
- 3.: Éter és benzin oldódás vízben, viselkedése jóddal VIDEÓ
- 4.: KI és KBr azonosítása VIDEÓ
- 5.: Sebbenzin, etilacetát, etanol azonosítása VIDEÓ
- 22.: Klórgáz előállítása sóoldat elektrolízissel, oxidáló hatása: VIDEÓ: elektrolízis, jodid oxidálása és kimutatása
- 29.: Bróm oldódása benzinben és NaOH-ban VIDEÓ
- 39.: Klórgáz előállítása, színtelenítő hatása VIDEÓ
- 53.: Brómos víz reakció szerves vegyületekkel - VIDEÓ